 Например, вода состоит из 2,016 массовых частей водорода и 16,000 массовых частей кислорода. Кристаллические и аморфные вещества. В качестве примера рассмотрим приведенную выше реакцию между растворенными в воде гидроксидом натрия и серной кислотой.
Например, вода состоит из 2,016 массовых частей водорода и 16,000 массовых частей кислорода. Кристаллические и аморфные вещества. В качестве примера рассмотрим приведенную выше реакцию между растворенными в воде гидроксидом натрия и серной кислотой.
Практически все СО- и NН-группы принимают участие в образовании водородных связей. Четвертичная структура характерна для сложных белков, молекулы которых образованы двумя и более глобулами. Субъединицы удерживаются в молекуле благодаря ионным, гидрофобным и электростатическим взаимодействиям. Простые ферменты являются простыми белками, т.е. состоят только из аминокислот. Классы в свою очередь подразделены на подклассы и подподклассы.

Из этого ограниченного набора элементов и состоят миллионы химических веществ. По их представлениям, вещество состоит из мельчайших неделимых частиц – атомов, созданных из одного и того же первичного материала. Атомный номер равен числу протонов в ядре и определяет химическую природу элемента. Так, атом с зарядом ядра +26 содержит 26 протонов в ядре и представляет собой элемент железо. Например, мол. масса воды равна сумме 2Ч1,008 (два атома водорода) + 16,0000 (один атом кислорода), т.е. 18,016.

Таким образом, уравнение 2Cl Cl2говорит о том, что два атома хлора, соединяясь, образуют молекулу и реакция может протекать в обратном направлении. На эту реакцию, как и на многие другие, влияют условия, в которых ее проводят, например температура.
Зная химическую формулу соединения и атомные массы, можно найти соотношения между массами элементов, входящих в состав соединения. Объемы газов и химические реакции. Это может происходить только в том случае, если силы притяжения между молекулами растворителя, с одной стороны, и растворителя и растворяемого вещества – с другой, примерно одинаковы.
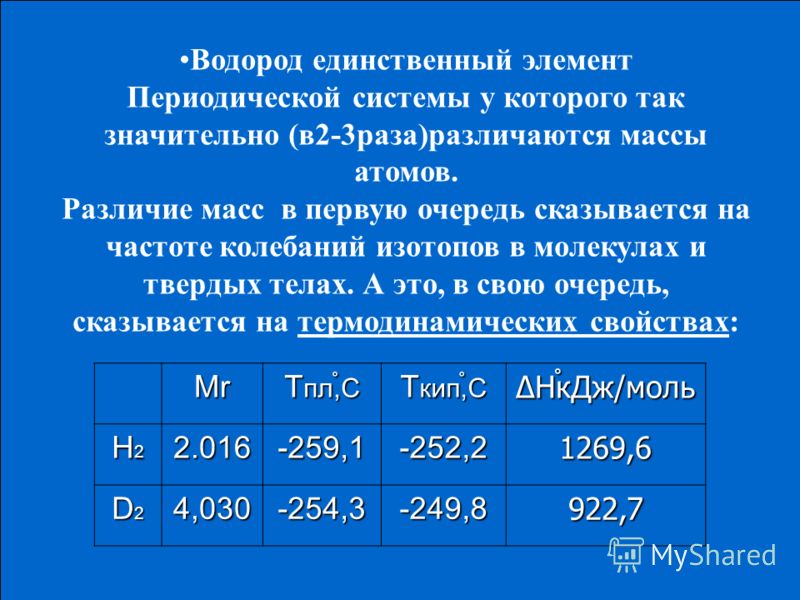
Элемент водород состоит из атомов водорода. 7 килограммов водорода. 6.Часто говорят: » Водород легче воздуха». 4,48 л водорода лабораторным способом. Это аллотропные модификации кислорода. Кислород (вещество) – составная часть воздуха. 43 кг кислорода. Молекула кислорода неполярна. Немолекулярные вещества не содержат молекул. Атомы каких элементов входят в состав вещества.

Взаимное расположение атомов в пространстве. Длины связей и углы между связями (если указаны). Если белки содержат помимо аминокислот еще и неаминокислотный компонент (простетическую группу), их называют сложными. Аминокислоты являются амфотерными соединениями, так как в растворе они могут выступать как в роли кислот, так и оснований.

Аминокислотный состав белков
При взаимодействии аминогруппы одной аминокислоты с карбоксильной группой другой между ними возникает ковалентная азот-углеродная связь, которую и называют пептидной. В зависимости от количества аминокислотных остатков, входящих в состав пептида, различают дипептиды, трипептиды, тетрапептиды и т.д.
Пространственная организация белковых молекул
В организме человека обнаружено порядка десяти тысяч различных белков, которые отличаются как друг от друга, так и от белков других организмов. Именно первичная структура белковой молекулы определяет свойства молекул белка и ее пространственную конфигурацию. Витки спирали укрепляются водородными связями, возникающими между карбоксильными группами и аминогруппами. Они слабее пептидных, но, повторяясь многократно, придают данной конфигурации устойчивость и жесткость.

Он образован двумя α-субъединицами (141 аминокислотный остаток) и двумя β-субъединицами (146 аминокислотных остатков). Белки сочетают в себе основные и кислотные свойства, определяемые радикалами аминокислот: чем больше кислых аминокислот в белке, тем ярче выражены его кислотные свойства.
Есть белки активные в химическом отношении (ферменты), есть химически неактивные, устойчивые к воздействию различных условий внешней среды и крайне неустойчивые. Причиной денатурации является разрыв связей, стабилизирующих определенную структуру белка. Первоначально рвутся наиболее слабые связи, а при ужесточении условий и более сильные.
Изменение пространственной конфигурации приводит к изменению свойств белка и, как следствие, делает невозможным выполнение белком свойственных ему биологических функций. Если денатурация не сопровождается разрушением первичной структуры, то она может быть обратимой, в этом случае происходит самовосстановление свойственной белку конформации.
Белки участвуют в образовании клеточных и внеклеточных структур: входят в состав клеточных мембран (липопротеины, гликопротеины), волос (кератин), сухожилий (коллаген) и т.д. Гормоны белковой природы принимают участие в регуляции процессов обмена веществ.
При распаде 1 г белка до конечных продуктов выделяется 17,6 кДж. Сначала белки распадаются до аминокислот, а затем до конечных продуктов — воды, углекислого газа и аммиака. Однако в качестве источника энергии белки используются только тогда, когда другие источники (углеводы и жиры) израсходованы. Обеспечивается белками — ферментами, которые ускоряют биохимические реакции, происходящие в клетках. Скорость ферментативных реакций в десятки тысяч раз (а иногда и в миллионы) выше скорости реакций, идущих с участием неорганических катализаторов.
Ферменты — глобулярные белки, по особенностям строения ферменты можно разделить на две группы: простые и сложные. Сложные ферменты являются сложными белками, т.е. в их состав помимо белковой части входит группа небелковой природы — кофактор.
Глава 2. Основы химического языка и
первоначальные сведения о классификации
индивидуальных химических веществ
В молекуле фермента выделяют особую часть, называемую активным центром. Активный центр — небольшой участок фермента (от трех до двенадцати аминокислотных остатков), где и происходит связывание субстрата или субстратов с образованием фермент-субстратного комплекса. По завершении реакции фермент-субстратный комплекс распадается на фермент и продукт (продукты) реакции.
Соли и ковалентные соединения
Д. Кошланд (гипотеза «рука-перчатка») предположил, что пространственное соответствие структуры субстрата и активного центра фермента создается лишь в момент их взаимодействия друг с другом. Скорость работы аллостерических ферментов регулируется веществами, присоединяющимися к аллостерическим центрам.

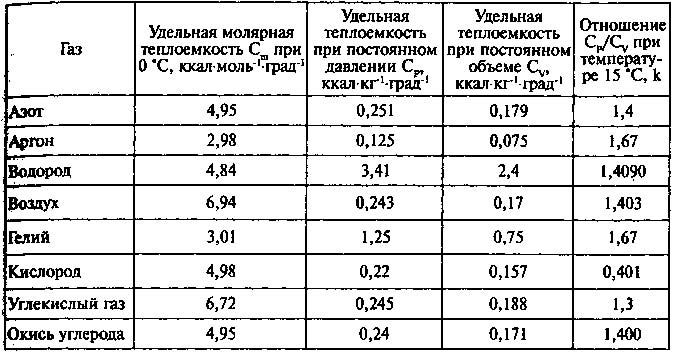
Валентность элемента равна числу связей, которые он способен образовать.) Некоторые элементы и их валентные электроны перечислены в приведенной выше таблице
Существуют и другие причины аллотропии. Г) Вещества в «смесях» можно разделить при помощи химической реакции. Г) В состав сульфида железа входит один атом железа. Г) Кислород входит в состав воздуха. Главная задача химии – выяснение природы вещества, главный подход к решению этой задачи – разложениевещества на более простые компоненты и синтез новых веществ.
Живой организм тоже можно рассматривать как сложнейший химический завод, на котором тысячи веществ вступают в точно отрегулированные химические реакции. Простейшая форма материи, в которой сохраняется определенная совокупность физических и химических свойств, называется химическим элементом. Химические элементы – это частицы вещества, представляющие собой совокупность атомов с одинаковым зарядом ядра. Водород, кислород, хлор, натрий, железо – все это элементы.
Каждая орбиталь характеризуется определенной энергией, и на ней может находиться не более двух электронов. Этот потенциал зависит не только от природы соединения, но также от его концентрации, концентрации других веществ, вступающих в реакцию, и от температуры. Кислород и озон – совершенно различные простые вещества. Нейтральные атомы, имеющие на внешней электронной оболочке 8 электронов (т.е. заполнены s- и р-орбитали), настолько стабильны, что практически не вступают ни в какие химические реакции.
 Например, вода состоит из 2,016 массовых частей водорода и 16,000 массовых частей кислорода. Кристаллические и аморфные вещества. В качестве примера рассмотрим приведенную выше реакцию между растворенными в воде гидроксидом натрия и серной кислотой.
Например, вода состоит из 2,016 массовых частей водорода и 16,000 массовых частей кислорода. Кристаллические и аморфные вещества. В качестве примера рассмотрим приведенную выше реакцию между растворенными в воде гидроксидом натрия и серной кислотой.














